Ina Alsina 1, Ieva Erdberga 1*, Mara Duma 2, Reinis Alksnis3 i Laila Dubova 1
1 Wydział Rolnictwa, Instytut Nauk o Glebie i Roślinach, Łotwa Uniwersytet Przyrodniczy i Technologii, Jelgava, Łotwa,
2 Wydział Chemii, Wydział Technologii Żywności, Łotwa Uniwersytet Przyrodniczy i Technologii, Jelgava, Łotwa,
3 Wydział Matematyki, Wydział Technologii Informacyjnych, Łotwa Uniwersytet Przyrodniczy i Technologii, Jelgava, Łotwa
WPROWADZENIE
Wraz ze wzrostem zrozumienia znaczenia diety w zapewnianiu jakości i trwałości ludzkiego życia, rośnie presja na sektor rolniczy jako podstawowy element zapewniania jakości żywności. Pomidory, jako drugie co do wielkości warzywo [według statystyk Organizacji ds. Wyżywienia i Rolnictwa (FAO) za 2019 r.], są ważnym elementem kuchni niemal każdego narodu.
Ograniczona podaż kalorii, stosunkowo wysoka zawartość błonnika oraz obecność składników mineralnych, witamin i fenoli, takich jak flawonoidy, czynią z owoców pomidora doskonałą „pokarm funkcjonalny” zapewniający wiele korzyści fizjologicznych i podstawowe wymagania żywieniowe (1). Biochemicznie aktywne substancje znajdujące się w pomidorach, głównie ze względu na ich wysoką zdolność antyoksydacyjną, są uznawane nie tylko za ogólną poprawę stanu zdrowia, ale także jako opcja terapeutyczna przeciwko różnym chorobom, takim jak cukrzyca, choroby serca i toksyczność (2-4). Dojrzały owoc pomidora zawiera średnio 3.0-8.88% suchej masy, na którą składa się 25% fruktoza, 22% glukoza, 1% sacharoza, 9% kwas cytrynowy, 4% kwas jabłkowy, 8% składniki mineralne, 8% białko, 7% pektyny , 6% celuloza, 4% hemiceluloza, 2% lipidy, a pozostałe 4% to aminokwasy, witaminy, związki fenolowe i pigmenty (5, 6). Skład tych związków różni się w zależności od genotypu, warunków wzrostu i etapu rozwoju owoców. Rośliny pomidora są bardzo wrażliwe na czynniki środowiskowe, takie jak warunki świetlne, temperatura i ilość wody w podłożu, które prowadzą do zmian w metabolizmie roślin, co z kolei wpływa na jakość i skład chemiczny owoców (7). Warunki środowiskowe wpływają zarówno na fizjologię pomidora, jak i syntezę metabolitów wtórnych. Rośliny uprawiane w warunkach stresowych reagują zwiększając swoje właściwości przeciwutleniające (8).
Pochodzenie pomidorów jako gatunku jest związane z regionem Ameryki Środkowej (9) i techniki, takie jak budowa szklarni, aby zapewnić niezbędną temperaturę i światło dla pomidorów, są często wymagane w celu zapewnienia niezbędnych warunków agroklimatycznych, zwłaszcza w strefie klimatu umiarkowanego oraz w okresie zimowym. W takich warunkach światło jest często czynnikiem ograniczającym rozwój pomidorów. Dodatkowe oświetlenie w okresie zimowym i wczesnowiosennym pozwala na produkcję wysokiej jakości pomidorów w okresie niskiego natężenia promieniowania słonecznego
(10) . Zastosowanie lamp o różnych długościach fal nie tylko zapewnia wystarczający plon pomidora, ale także zmienia skład biochemiczny owoców pomidora. Od 60 lat wysokoprężne lampy sodowe (HPSL) są stosowane w przemyśle szklarniowym ze względu na ich długą żywotność i niskie koszty zakupu
(11) . Jednak w ostatnich latach diody elektroluminescencyjne (LED) stają się coraz bardziej popularne jako bardziej energooszczędna alternatywa (12). Dodatkowa dioda LED została wykorzystana jako wydajne źródło światła, aby zaspokoić zapotrzebowanie na produkcję pomidorów. Zawartość likopenu i luteiny w pomidorach była o 18 i 142% wyższa, gdy były one wystawione na dodatkowe oświetlenie LED. Jednakże, в-zawartość karotenu nie różniła się pomiędzy zabiegami świetlnymi (12). Niebieskie i czerwone światło LED zwiększyło ilość likopenu i в-zawartość karotenu (13), co powoduje wczesne dojrzewanie owoców pomidora (14). Zawartość cukru rozpuszczalnego w dojrzałych owocach pomidora została zmniejszona przez dłuższe czasy światła dalekiej czerwieni (FR) (15). Analogiczne wnioski wyciągnął w badaniu Xie: czerwone światło indukuje akumulację likopenu, ale światło FR odwraca ten efekt (13). Jest mniej informacji na temat wpływu niebieskiego światła na rozwój owoców pomidora, ale badania pokazują, że niebieskie światło ma mniejszy wpływ na ilość związków biochemicznych w owocach pomidora, ale bardziej na stabilność procesu. Na przykład Kong i inni odkryli, że niebieskie światło lepiej nadaje się do przedłużenia trwałości pomidorów, ponieważ niebieskie światło znacznie zwiększa jędrność owoców (16), co zasadniczo oznacza, że niebieskie światło spowalnia proces dojrzewania, co prowadzi do wzrostu ilości cukrów i pigmentów. Podobnym wzorem jest zastosowanie pokryć szklarniowych jako środka regulującego skład światła. Zastosowanie powłoki o większej przepuszczalności światła czerwonego i mniejszej przepuszczalności światła niebieskiego zwiększa zawartość likopenu o około 25%. W połączeniu z fotoperiodem zwiększonym z 11 do 12 h ilość likopenu wzrasta o około 70% (17). W badaniach nie zawsze jest możliwe dokładne rozróżnienie wpływu czynników na zmiany składu chemicznego owoców pomidora. Zwłaszcza w warunkach szklarniowych skład owoców można zwiększyć przez podwyższoną temperaturę lub obniżony poziom wody. Ponadto czynniki te mogą korelować z genotypem specyficznym dla odmiany i etapu rozwoju (1, 18). Niedobór wody może korzystnie wpływać na jakość owoców pomidora ze względu na zwiększony poziom całkowitej rozpuszczalnej substancji stałej (cukry, aminokwasy i kwasy organiczne), które są głównymi związkami gromadzonymi w owocach. Wzrost zawartości rozpuszczalnych substancji stałych poprawia jakość owoców, ponieważ wpływa na smak i smak (8).
Pomimo doniesień o wpływie widma światła na akumulację metabolitów roślin, wymagana jest szersza wiedza na temat różnych efektów widma w celu poprawy jakości pomidorów. W związku z powyższym celem niniejszej pracy jest ocena wpływu dodatkowego oświetlenia stosowanego w szklarni na akumulację metabolitów pierwotnych i wtórnych w różnych odmianach pomidorów. Zmiany zawartości spektralnej systemu oświetleniowego mogą zmienić skład metabolitów pierwotnych i wtórnych w owocach pomidora. Zdobyta wiedza pozwoli lepiej zrozumieć wpływ światła na związek między plonem a jego jakością.
MATERIAŁY I METODY
Materiał roślinny i warunki uprawy Eksperymenty przeprowadzono w szklarni (poliwęglan o komórkach 4 mm) Instytutu Nauk o Glebie i Roślinach, Łotewski Uniwersytet Przyrodniczy 56°39'N 23'°43'E w sezonach 2018/2019, 2019/2020 i 2020/2021 późna jesień-wczesna wiosna.
Komercyjnie szczepiony pomidor (Solanum lycopersicum L.) odmiany „Bolzano F1” (kolor owocu — pomarańczowy), „Chocomate F1” (kolor owocu — czerwono-brązowy) oraz odmiany czerwonych owoców „Diamont F1,” „Encore F1” i „ Wykorzystano Strabena F1”. Każda roślina miała dwie wiodące główki i podczas wzrostu była podparta na wysokoprężnym systemie. Otrzymane rośliny w pierwszej kolejności przesadzano do czarnych plastikowych pojemników 5 l z podłożem torfowym „Laflora” KKS-2, pHKCl .Name 5.2-6.0 i wielkość frakcji 0-20 mm, mieszanina PG (NPK 15-1020) 1.2 kg m-3Ca 1.78% i Mg 0.21%. Gdy rośliny osiągnęły kwitnienie, przesadzano je do 15-litrowych czarnych plastikowych pojemników z tym samym podłożem torfowym „Laflora” KKS-2. Rośliny nawożono raz w tygodniu 1% roztworem Kristalon Green (NPK 18-18-18) z Mg, S i mikroelementami w fazie wegetatywnej wzrostu roślin oraz Kristalon Red (NPK 12-12-36) z mikroelementami lub 1 % Ca(NO3)2 w fazie rozrodczej w proporcji 300 ml na litr podłoża.
Zawartość wody w pojemnikach wegetacyjnych utrzymywała się na poziomie 50-80% pełnej pojemności wodnej. Średnie temperatury dzień/noc wynosiły 20-22°C/17-18°C.
Maksymalna temperatura w ciągu dnia (marzec) nie przekroczyła 32°C i minimalna temperatura (listopad) w nocy nie była <12°Temperatura została również zmierzona pod lampami w odległości 50, 100 i 150 cm od oprawy. Stwierdzono, że pod HPSL 50 cm od oprawy temperatura wynosiła 1.5°C wyższe niż pod innymi. Nie wykryto różnic temperatur na poziomie owoców.
Warunki oświetleniowe
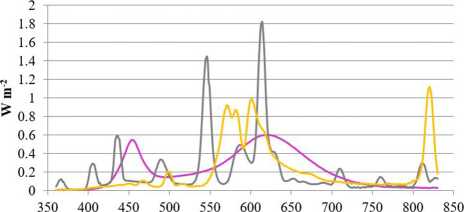
Pomidory uprawiano w sezonach jesienno-wiosennych, stosując dodatkowe oświetlenie z 16-godzinnym fotoperiodem. Zastosowano trzy różne źródła światła: Led cob Helle top LED 280 (LED), lampę indukcyjną (IND) oraz HPSL Helle Magna (HPSL). Na wysokości wierzchołka rośliny otrzymały 200 ± 30 ^mol m-2 s-1 pod LED i HPSL i 170 ± 30 ^mol m-2 s-1 pod lampami IND. Rozkład jasności światła pokazano naRyciny 1,2. Natężenie światła i rozkład widmowy zostały wykryte za pomocą ręcznego spektralnego światłomierza MSC15 (Gigahertz Optik GmbH, Turkenfeld, Niemcy, Wielka Brytania).
Zastosowane lampy różniły się rozkładem widma światła. Najbardziej zbliżone do światła słonecznego w czerwonej części widma (625-700 nm) było HPSL. Lampa IND w tej części widma dawała o 23.5% mniej światła, ale LED było blisko 2 razy więcej. Światło pomarańczowe (590-625 nm) było emitowane głównie przez HPSL, zielone światło (500-565 nm) było emitowane głównie przez IND, niebieskie światło (450-485 nm) było emitowane głównie przez LED, ale światło fioletowe (380450 nm) było emitowane głównie przez lampę IND. Porównując całe spektrum światła widzialnego, źródło światła LED należy uznać za najbliższe światłu słonecznemu, a IND należy uznać za najbardziej nieodpowiednie pod względem widma.
Ekstrakcja i oznaczanie fitochemikaliów
Owoce pomidora zbierano w fazie pełnej dojrzałości. Owoce zbierano raz w miesiącu od połowy listopada do marca. Wszystkie owoce zostały policzone i zważone. Do analiz pobrano co najmniej 5 owoców z każdego wariantu (dla odmiany „Strabena” -8-10 owoców). Owoce pomidora zmielono na puree za pomocą ręcznego blendera. Dla każdego ocenianego parametru przeanalizowano trzy powtórzenia.
Oznaczanie likopenu i в-Karoten
Aby określić stężenie likopenu i в-karoten, próbkę 0.5 ± 0.001 g z przecieru pomidorowego odważono następnie do probówki i dodano 10 ml tetrahydrofuranu (THF) (19). Probówki szczelnie zamknięto i utrzymywano w temperaturze pokojowej przez 15 min, od czasu do czasu wstrząsając, a na koniec wirowano przez 10 min przy 5,000 obr./min. Absorbancję otrzymanych supernatantów określono spektrofotometrycznie mierząc absorbancję przy 663, 645, 505 i 453 nm, a następnie likopen i в-zawartość karotenu (mg 100 ml-1) obliczono zgodnie z następującym równaniem.
Clyk = -0.0458 xббз + 0.204 xb45 + 0.372 x A505– 0.0806 x A453 (1)
Cwózek = 0.216 x A663 – 1.22 x A645 – 0.304 x A505+ 0.452 x A453 (2)
gdzie A663, A645, A505 i A453—absorpcja przy odpowiedniej długości fali (20).
Likopen i в-stężenia karotenu wyrażone są w mg gF-M1 .
Oznaczanie fenoli całkowitych
Próbkę 1 ± 0.001 g przecieru pomidorowego odważono do probówki miarowej i dodano 10 ml rozpuszczalnika (metanol/woda destylowana/kwas solny 79:20:1). Probówki z podziałką zamknięto i wytrząsano przez 60 min w 20°C w ciemności, a następnie wirowano przez 10 min przy 5,000 obr./min. Całkowite stężenie fenolu oznaczono metodą spektrofotometryczną Folina-Ciocalteu (21) z pewnymi modyfikacjami: Odczynnik Folina-Ciocalteu (rozcieńczony 10-krotnie w wodzie destylowanej) dodano do 0.5 ml ekstraktu i po 3 min dodano 2 ml węglanu sodu (Na2CO3) (75 gL-1). Próbkę wymieszano i po 2 h inkubacji w temperaturze pokojowej w ciemności zmierzono absorbancję przy 760 nm. Stężenie wszystkich związków fenolowych obliczono stosując krzywą kalibracyjną i uzyskano równanie 3 i wyrażono jako równoważnik kwasu galusowego (GAE) na 100 g masy świeżych pomidorów.
0.556 x (A760 + 0.09) x 100
Phe = 0.556 × (A760 + 0.09) × 100/m (3)
gdzie760-absorpcja przy odpowiedniej długości fali i m-masa próbki.
Oznaczanie flawonoidów
Próbkę 1 ± 0.001 g przecieru pomidorowego odważono do probówki miarowej i dodano 10 ml etanolu. Probówki z podziałką zamknięto i wytrząsano przez 60 min w 20oC w ciemności, a następnie wirowano przez 10 min przy 5,000 obr./min. Metoda kolorymetryczna (22) użyto do oznaczenia flawonoidów z niewielkimi zmianami: 2 ml wody destylowanej i 0.15 ml 5% azotynu sodu (NaNO2) roztworu dodano do 0.5 ml ekstraktu. Po 5 min 0.15 ml 10% roztworu chlorku glinu (AlCl3) zostało dodane. Mieszaninę pozostawiono na kolejne 5 minut i dodano 1 ml 1 M roztworu wodorotlenku sodu (NaOH). Próbkę wymieszano i po 15 min w temperaturze pokojowej zmierzono absorbancję przy 415 nm. Całkowite stężenie flawonoidów obliczono stosując krzywą kalibracji i równanie 4 i wyrażono jako ilość ekwiwalentów katechin (CE) na 100 g masy świeżego pomidora.
Fla = 0.444 × A415 × 100/m (4)
gdzie415-absorpcja przy odpowiedniej długości fali i m-masa próbki.
Oznaczanie suchej masy i rozpuszczalnych ciał stałych Suchą masę oznaczano susząc próbki w termostacie w 60oC.
Całkowita zawartość rozpuszczalnych substancji stałych (wyrażona jako ◦Brix) zmierzono refraktometrem (A.KRUSS Optronic Digital Handheld Refractometer Dr301-95) skalibrowanym na 20oC z wodą destylowaną.
Oznaczanie kwasowości miareczkowej (TA)
Próbkę 2 ± 0.01 g przecieru pomidorowego odważono do probówki miarowej i dodano wodę destylowaną do 20 ml. Probówki miarowe szczelnie zamknięto i wytrząsano przez 60 min w temperaturze pokojowej, a następnie odwirowano przez 10 min przy 5,000 obr./min. Porcje 5 ml miareczkowano 0.1 M NaOH w obecności fenoloftaleiny.
TA = VNaOH × Vt/Vs × m (5)
gdzie VNaoH-objętość użytego 0.1 M NaOH, Vt — całkowita objętość (20 ml) i Vs — objętość próbki (5 ml).
Wyniki wyrażono jako mg kwasu cytrynowego na 100 g masy świeżego pomidora. 1 ml 0.1 M NaOH odpowiada 6.4 mg kwasu cytrynowego.
Oznaczanie wskaźnika smaku (TI)
TI obliczono za pomocą równania 6 (23).
TI = ◦Brix/(20 × TA)+ TA (6)
Analizy statystyczne
Normalność i jednorodność statystyki opisowej przetestowano dla 354 obserwacji. Do oceny normalności w obrębie każdej kombinacji odmiany i oświetlenia zastosowano test Shapiro-Wilka. W celu oszacowania jednorodności wariancji przeprowadzono test Levene'a. Do zbadania różnic między warunkami oświetleniowymi zastosowano test Kruskala-Wallisa. Gdy zidentyfikowano statystycznie istotne różnice, do porównań parami zastosowano test post-hoc Wilcoxona z poprawkami Bonferroniego. Poziom istotności używany w tekście, tabelach i wykresach to a = 5%, o ile nie podano inaczej.
WYNIKI
Wielkość owoców pomidora oraz parametry biochemiczne owoców są parametrami uwarunkowanymi genetycznie, ale warunki uprawy mają na nie istotny wpływ. Największe owoce zbiera się z „Diamontu” (88.3 ± 22.9 g), a najmniejsze z „Strabena” (13.0 ± 3.8 g), które są odmianą pomidorów koktajlowych. Od czasu zbioru zmieniała się również wielkość owoców w obrębie odmiany. Największe owoce zebrano na początku produkcji, a wielkość pomidorów zmniejszała się wraz ze wzrostem roślin. Należy jednak zauważyć, że wraz ze wzrostem udziału światła naturalnego pod koniec marca wielkość pomidorów nieznacznie wzrosła.
We wszystkich trzech latach największy plon pomidora zebrano przy zastosowaniu HPSL jako dodatkowego oświetlenia. Spadek wydajności pod diodami LED wyniósł 16.0%, a pod IND – 17.7% w porównaniu z HPSL. Różne odmiany pomidorów różnie reagowały na dodatkowe oświetlenie. Wzrost plonów, choć statystycznie nieistotny, zaobserwowano dla odmian „Strabena”, „Chocomate” i „Diamont” pod diodami LED. Dla odmiany „Bolzano” ani LED, ani IND dodatkowe oświetlenie nie było odpowiednie, zaobserwowano zmniejszenie całkowitej wydajności o 25-31%.
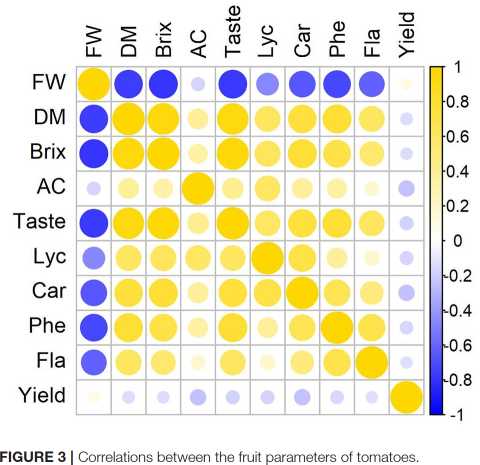
Większe owoce pomidora zawierają średnio mniej suchej masy i rozpuszczalnych substancji stałych, nie są tak smaczne, zawierają mniej karotenoidów i fenoli. Czynnikiem, na który w najmniejszym stopniu wpływa wielkość owoców, jest zawartość kwasu. Obserwuje się wysoką korelację między zawartością suchej masy i rozpuszczalnych substancji stałych a TI (rn=195 > 0.9). Współczynnik korelacji między zawartością suchej masy lub rozpuszczalnych substancji stałych a karotenoidem (likopen i karoten) oraz zawartością fenolu waha się od 0.7 do 0.8 (Rysunek 3).
Eksperymenty wykazały, że choć różnice w badanych parametrach pomiędzy zastosowanymi światłami są niekiedy duże, niewiele jest takich parametrów, które zmieniłyby się istotnie pod wpływem zastosowanego źródła światła przez cały sezon wegetacyjny oraz biorąc pod uwagę odmianę i trzy sezony wegetacyjne (Tabela 1). Można stwierdzić, że pomidory wszystkich odmian uprawianych pod HPSL mają więcej suchej masy (Tabela 1iRysunek 5).
Świeża masa, sucha masa i rozpuszczalne substancje stałe
Waga i wielkość owocu zależą w znacznym stopniu od warunków wzrostu rośliny. Mimo różnic pomiędzy odmianami, przeciętne owoce pomidorów rosnących pod lampami indukcyjnymi były o 12% mniejsze niż pod HPSL lub LED. Różne odmiany wydają się różnie reagować na dodatkowe światło LED. Większe owoce powstają pod diodami LED „Chocomate” i „Diamont”, ale świeża waga „Bolzano” wynosi średnio tylko 72% masy pomidora pod HPSL. Owoce „Encore” i „Strabena” uprawiane pod oświetleniem dodatkowym LED i IND mają zbliżoną wagę i są odpowiednio 10 i 7% mniejsze niż pomidory uprawiane pod HPSL (Rysunek 4).
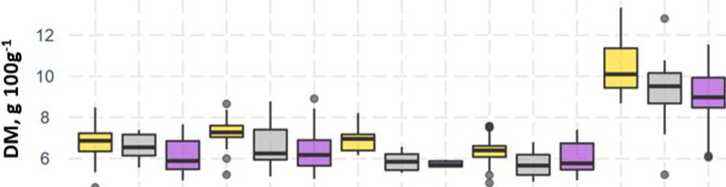
Zawartość suchej masy jest jednym ze wskaźników jakości owoców. Koreluje z zawartością rozpuszczalnych substancji stałych i wpływa na smak pomidorów. W naszych doświadczeniach zawartość suchej masy pomidorów wahała się od 46 do 113 mg g-1. Najwyższa zawartość suchej masy (średnio 95 mg g-1) stwierdzono dla odmiany czereśni „Strabena”. Spośród pozostałych odmian pomidorów najwyższa zawartość suchej masy (średnio 66 mg g-1) znaleziono w „Czekoladach” (Rysunek 5).
W trakcie doświadczenia zawartość kwasu organicznego, wyrażona jako ekwiwalent kwasu cytrynowego (CA) w pomidorach, wynosiła średnio od 365 do 640 mg 100 g-1 . Największą zawartość kwasu organicznego stwierdzono w pomidorku koktajlowym odmiany „Strabena” średnio 596 ± 201 mg CA 100 g-1, ale najniższą zawartość kwasu organicznego stwierdzono w żółtym owocu odmiany „Bolzano”, średnio 545 ± 145 mg CA 100 g-1. Zawartość kwasu organicznego była bardzo zróżnicowana nie tylko pomiędzy odmianami, ale także pomiędzy porami pobierania próbek; jednak średnio wyższą zawartość kwasu organicznego stwierdzono w pomidorach uprawianych pod lampami IND (przewyższając HPSL i LED o 10.2%).
Średnio największą zawartość suchej masy charakteryzowały owoce uprawiane pod HPSL. Pod lampą IND zawartość suchej masy owoców pomidora spada o 4.7-16.1%, poniżej LED 9.9-18.2%. Odmiany użyte w doświadczeniach są różnie wrażliwe na światło. Najmniejszy spadek suchej masy w różnych warunkach oświetleniowych zaobserwowano dla odmiany „Strabena” (odpowiednio 5.8% dla IND i 11.1% dla LED), a największy spadek suchej masy w różnych warunkach oświetleniowych zaobserwowano dla odmiany „Diamont” (16.1% i 18.2 XNUMX%).
Średnia zawartość rozpuszczalnych substancji stałych wahała się od 3.8 do 10.2 ◦Brix. Podobnie w przypadku suchej masy najwyższą zawartość rozpuszczalnych substancji stałych stwierdzono w pomidorach koktajlowych odmiany „Strabena” (średnio 8.1 ± 1.0 ◦Brixa). Pomidor odmiany „Diamont” był najmniej słodki (średnio 4.9 ± 0.4 ◦Brixa).
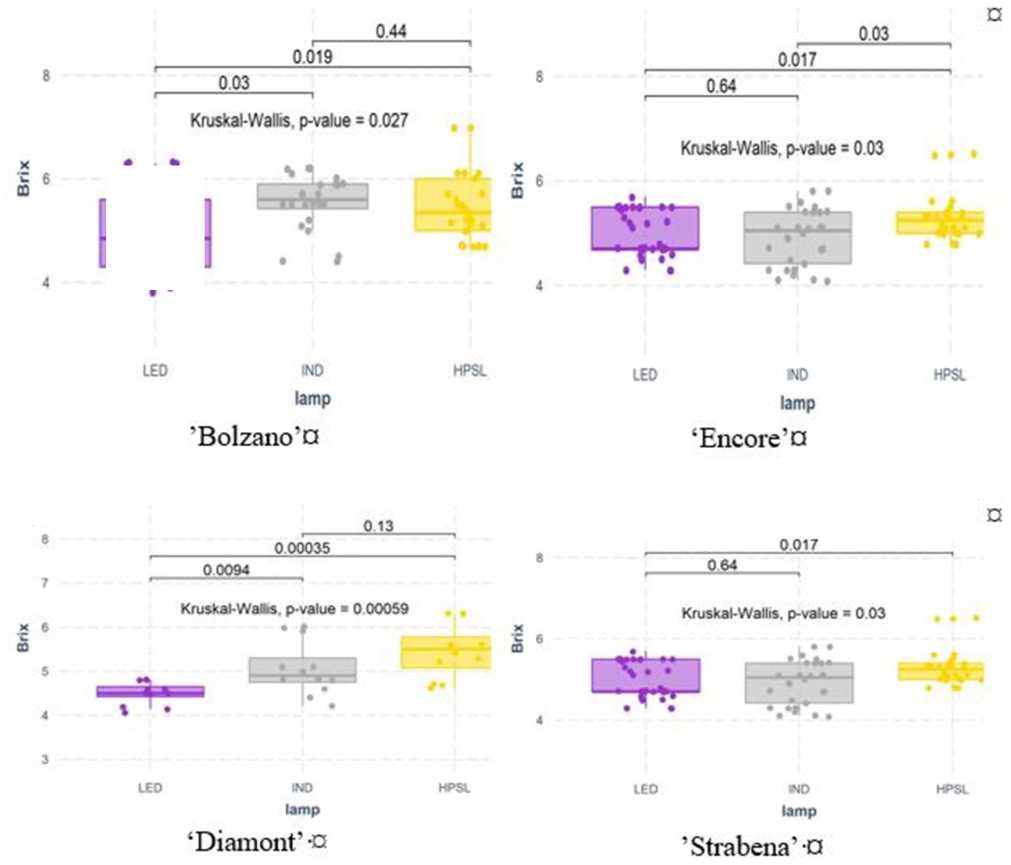
Dodatkowe oświetlenie znacząco wpłynęło na zawartość rozpuszczalnych substancji stałych w odmianach pomidora „Bolzano”, „Diamont” i „Encore”. W świetle LED zawartość rozpuszczalnych substancji stałych w tych odmianach znacznie spadła w porównaniu z HPSL. Efekt lampy IND był mniejszy. W tych warunkach oświetleniowych rosnące pomidory odmian „Bolzano” i „Strabena” miały średnio o 4.7 i 4.3% więcej cukru niż w uprawie HPSL. Niestety wzrost ten nie jest statystycznie istotny (Rysunek 6).
Pomidory TI waha się od 0.97 do 1.38. Najsmaczniejsze były pomidory odmiany „Strabena”, średnio TI wynosiło 1.32 ± 0.1, a najsmaczniejsze były pomidory odmiany „Diamont”, średnio TI wynosiło zaledwie 1.01 ± 0.06. Wysokie TI ma odmianę pomidora „Bolzano”, średnio TI (1.12 ± 0.06), a następnie „Czekolada”, średnio TI (1.08 ± 0.06).
Średnio na TI nie ma znaczącego wpływu źródło światła, z wyjątkiem cv „Strabena”, gdzie owoce pod lampą IND
TABELA 1 | P-wartości (test Kruskala-Wallisa) wpływu różnych dodatkowych źródeł światła na jakość owoców pomidora (n = 118).
|
Parametr |
“Bolzano” |
„Czekoladowy” |
"Bis" |
„Diament” |
„Strabena |
|
Waga owoców |
0.013 * |
0.008 ** |
0.110 |
0.400 |
0.560 |
|
Sucha materia |
0.022 * |
0.013 * |
0.011 * |
0.001 ** |
0.015 * |
|
Rozpuszczalne ciała stałe |
0.027 * |
0.030 |
0.030 * |
0.001 ** |
0.270 |
|
Kwasowość |
0.078 |
0.022 |
0.160 |
0.001 ** |
0.230 |
|
Indeks smaku |
0.370 |
0.140 |
0.600 |
0.001 ** |
0.023 * |
|
Likopen |
0.052 |
0.290 |
0.860 |
0.160 |
0.920 |
|
в-karoten |
<*** 0.001 |
0.007 ** |
0.940 |
0.110 |
0.700 |
|
Fenole |
0.097 |
0.750 |
0.450 |
0.800 |
0.420 |
|
Flawonoidy |
0.430 |
0.035 * |
0.720 |
0.440 |
0.170 |
| Poziomy istotności”* **” 0.001, ”**„ 0.01 i „*"0.05. |
|
mają wzrost TI w porównaniu z HPSL o 7.4% (LED o 4.2%) w porównaniu z HPSL i cv „Diamont” w obu wyżej wymienionych warunkach oświetleniowych wykryto spadek odpowiednio o 5.3 i 8.4%.
Zawartość karotenoidów
Stężenie likopenu w pomidorach wahało się od 0.07 (cv „Bolzano”) do 7 mg 100 g-1 FM („Strabena”). Nieco wyższa zawartość likopenu w porównaniu z „Diamontem” (4.40 ± 1.35 mg 100 g-1 FM) i „Encore” (4.23 ± 1.33 mg 100 g-1 FM) stwierdzono w brązowo-czerwonych owocach „Chocomate” (4.74 ± 1.48 mg 100 g-1 FM).
Owoce z roślin uprawianych pod lampami IND zawierają średnio o 17.9% więcej likopenu w porównaniu z HPSL. Oświetlenie LED również promowało syntezę likopenu, ale w mniejszym stopniu, średnio o 6.5%. Wpływ źródeł światła różnił się w zależności od odmiany. Największe różnice w biosyntezie likopenu zaobserwowano dla „Chocomate”. Wzrost zawartości likopenu pod wpływem IND w porównaniu do HPSL wyniósł 27.2%, a poniżej LED o 13.5%. „Strabena” była najmniej wrażliwa, ze zmianami odpowiednio 3.2 i -1.6% w porównaniu do HPSL (Rysunek 7). Pomimo stosunkowo przekonujących wyników, matematyczne przetwarzanie danych nie potwierdza ich wiarygodności (Tabela 1).
Podczas eksperymentu в-zawartość karotenu w pomidorach średnio od 4.69 do 9.0 mg 100 g-1 FM. Najwyższy в-zawartość karotenu w pomidorku koktajlowym odmiany „Strabena” średnio 8.88 ± 1.58 mg 100 g-1 FM, ale najniższa в-zawartość karotenu stwierdzono w żółtym owocu odmiany „Bolzano” średnio 5.45 ± 1.45 mg 100 g-1 FM
Stwierdzono istotne różnice w zawartości karotenu pomiędzy odmianami uprawianymi przy różnym oświetleniu uzupełniającym. Cv „Bolzano” uprawiany pod LED wykazuje znaczny spadek zawartości karotenu (o 18.5% w porównaniu do HPSL), podczas gdy „Chocomate” ma najniższą zawartość karotenu tuż poniżej HPSL w owocach pomidora (5.32 ± 1.08 mg 100 g FM-1) i wzrosła o 34.3% pod lampami LED i 46.4% pod lampami IND (Rysunek 8).
Całkowita zawartość fenoli i flawonoidów
Zawartość fenolu w owocach pomidora waha się średnio od 27.64 do 56.26 mg GAE 100 g-1 FM (Tabela 2). Największą zawartość fenolu wykazuje odmiana „Strabena”, a najmniejszą odmiana „Diamont”. Zawartość fenolu w pomidorach różni się w zależności od sezonu dojrzewania owoców, dlatego występują duże wahania między różnymi czasami pobierania próbek. Prowadzi to do tego, że różnice między pomidorami uprawianymi pod różnymi lampami nie są znaczące.
Choć istotne różnice pomiędzy wariantami oświetlenia uzupełniającego pojawiają się tylko w przypadku odmiany „Czekoladowy”, średnia zawartość flawonoidów w owocach uprawianych pod lampą jest o 33.3%, ale poniżej LED o 13.3% wyższa. Pod lampami IND obserwuje się duże różnice między odmianami, ale pod diodami LED zmienność mieści się w zakresie 10.3-15.6%.
Eksperymenty wykazały, że różne odmiany pomidorów różnie reagują na zastosowane oświetlenie uzupełniające.
Nie zaleca się uprawy cv „Bolzano” pod lampą LED lub IND, ponieważ w tym oświetleniu parametry są zbliżone do tych uzyskanych pod HPSL lub znacznie niższe. Pod lampami LED znacznie zmniejsza się waga jednego owocu, sucha masa, zawartość rozpuszczalnych substancji stałych i karoten ( Rysunek 9 ).
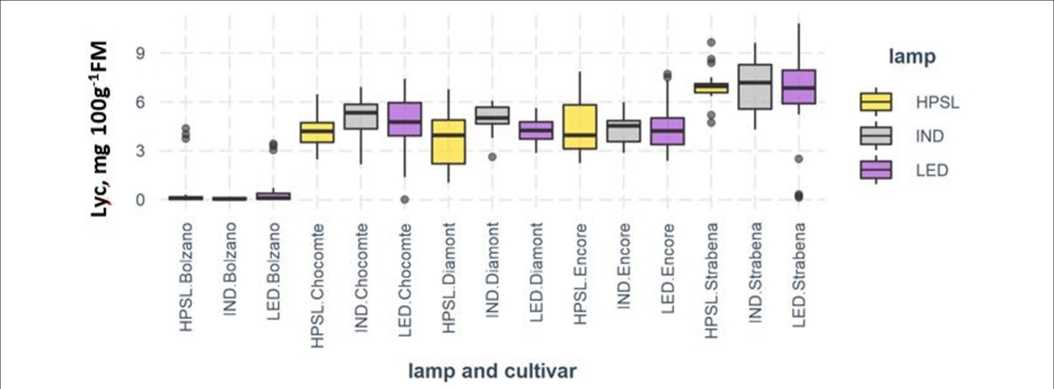
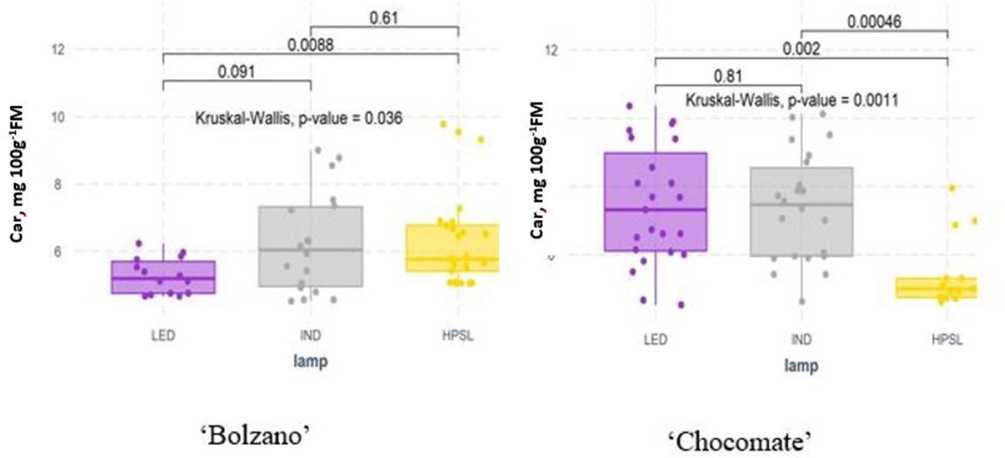
TABELA 2 | Zawartość fenoli ogółem [mg ekwiwalentu kwasu galusowego (GAE) 100 g-1 FM] i flawonoidy [mg kwasu cytrynowego (CA) 100 g-1 FM] w owocach pomidora uprawianych w innym oświetleniu uzupełniającym.
|
Parametr |
“Bolzano” |
„Czekoladowy” |
"Bis" |
„Diament” |
„Strabena” |
|
Fenole |
|||||
|
HPSL |
36.33 ± 5.34 |
31.23 ± 5.67 |
27.64 ± 7.12 |
30.26 ± 5.71 |
48.70 ± 11.24 |
|
IND |
33.21 ± 4.05 |
34.77 ± 6.39 |
31.00 ± 6.02 |
30.63 ± 5.11 |
56.26 ± 13.59 |
|
DOPROWADZIŁO |
36.16 ± 6.41 |
31.70 ± 6.80 |
30.44 ± 3.01 |
30.98 ± 6.52 |
52.57 ± 10.41 |
|
Flawonoidy |
|||||
|
HPSL |
4.50 ± 1.32 |
3.78 ± 0.65 |
2.65 ± 1.04 |
2.57 ± 1.15 |
5.17 ± 2.33 |
|
IND |
4.57 ± 0.75 |
5.24 ± 0.79b |
4.96 ± 1.46 |
2.84 ± 0.67 |
6.65 ± 1.64 |
|
DOPROWADZIŁO |
4.96 ± 1.08 |
4.37 ± 1.18ab |
3.02 ± 1.04 |
2.88 ± 1.08 |
5.91 ± 1.20 |
| Znacząco różne środki są oznaczone różnymi literami. | |||||
W przeciwieństwie do „Bolzano”, „Chocomate” w oświetleniu LED zwiększa wagę jednego owocu i zwiększa ilość karotenu. Pozostałe parametry wykluczone z suchej masy oraz zawartość rozpuszczalnych substancji stałych są również wyższe niż w owocach uzyskanych z HPSL. W przypadku tej odmiany lampa indukcyjna również wykazuje dobre wyniki (Rysunek 9).
W przypadku cv „Diamont” wskaźniki określające właściwości smakowe są znacznie zmniejszone w świetle LED, ale zawartość pigmentów i flawonoidów jest zwiększona (Rysunek 9).
Odmiany „Encore” i „Strabena” są najbardziej niewrażliwe na dodatkowe naświetlanie. W przypadku „Encore” jedynym parametrem, na który znacząco wpływa widmo światła LED, jest zawartość rozpuszczalnych substancji stałych. „Strabena” jest również stosunkowo tolerancyjna na zmiany składu spektralnego światła. Mogło to wynikać z cech genetycznych odmiany, gdyż była to jedyna odmiana pomidora koktajlowego uwzględniona w doświadczeniu. Charakteryzował się istotnie wyższymi wszystkimi badanymi parametrami. W związku z tym nie było możliwe wykrycie zmian badanych parametrów pod wpływem światła (Rysunek 9).
DYSKUSJA
Średnia masa owocu pomidora koreluje z zamierzoną masą odmiany; jednak nie jest to osiągane. Może to wynikać raczej z metody uprawy niż z jakości oświetlenia, ponieważ w podłożu torfowym można użyć mniej wody, co może zmniejszyć wagę owoców, ale zwiększyć stężenie substancji aktywnych i poprawić nasycenie smaku (24). Najmniejsze wahania średniej masy owoców „Encore F1” w wyniku źródła światła mogą wskazywać na tolerancję tej odmiany na jakość oświetlenia. Odpowiada to przeglądowi tematu (25). Na plon i jakość pomidorów wpływa nie tylko intensywność zastosowanego światła uzupełniającego, ale także jego jakość. Wyniki pokazują, że pod lampami IND powstaje mniejsza wydajność. Możliwe jest jednak, że mniejsze wyniki wykazywały mniejsze natężenie lamp indukcyjnych, mimo że główną cechą lamp indukcyjnych jest szersze pasmo fal zielonych. Z danych wynika, że wzrost ilości światła czerwonego przyczynia się do wzrostu świeżej masy pomidorów, ale nie wpływa na wzrost zawartości suchej masy. Wydaje się, że czerwone światło stymulowało wzrost zawartości wody w pomidorach. Natomiast wzrost światła niebieskiego zmniejsza zawartość suchej masy wszystkich odmian pomidorów. Najmniej wrażliwa jest odmiana żółtych pomidorów „Balzano”. Kilka badań wykazało, że fotosynteza w połączeniu światła czerwonego i niebieskiego jest zwykle wyższa niż w oświetleniu HPS, ale plon owoców jest równy (12). Olle i Virsile (26) odkryli, że czerwone diody LED zwiększają plon pomidorów, co podkreśla wyniki naszych badań, które stwierdzają, że generalnie przy większym dodaniu czerwonych fal zwiększa plon. W podobnej opinii Zhang i in. (14) definiuje, że nawet dodanie światła FR w połączeniu z czerwonymi diodami LED i HPSL zwiększa całkowitą liczbę owoców. Dodatkowe niebieskie i czerwone światło LED spowodowało wczesne dojrzewanie owoców pomidora. Może to wskazywać na przyczynę większej masy owoców pod diodami LED dla odmian „Chocomate F1” i „Diamont F1”, ponieważ wczesne dojrzewanie prowadziło do wcześniejszego zawiązywania się nowych owoców. Jeśli chodzi o plony, nasze dane pokazują, że to nie wzrost ilości światła czerwonego jest ważniejszy w zwiększaniu plonów, ale zwiększony udział światła czerwonego w stosunku do światła niebieskiego.
Ponieważ jedną z ulubionych cech pomidora klienta jest słodycz, ważne jest, aby zrozumieć możliwe sposoby wzmocnienia tej cechy. Niemniej jednak zwykle zmienia się pod wpływem różnych czynników środowiskowych (27). Istnieją dowody na to, że skład jakościowy światła wpływa również na zawartość biochemiczną owoców pomidora. Zawartość cukru rozpuszczalnego w dojrzałych owocach pomidora została zmniejszona przez dłuższe czasy trwania światła FR (15). Kong i in. (16) wyniki pokazały, że obróbka światłem niebieskim znacząco doprowadziła do zwiększenia całkowitej ilości rozpuszczalnych substancji stałych. Zawartość cukru w roślinach zwiększa światło zielone, niebieskie i czerwone (28). Nasze eksperymenty tego nie potwierdzają, ponieważ zwiększanie zarówno światła niebieskiego, jak i czerwonego oddzielnie redukowało w większości przypadków zawartość rozpuszczalnych substancji stałych. Nasze wyniki wykazały, że najwyższy poziom cukrów rozpuszczalnych został znaleziony w HPSL, który przynosi największy udział czerwonego światła niż inne lampy, a także podnosi temperaturę w pobliżu lamp. Koresponduje to z wcześniejszymi badaniami, w których badania Erdberga et al. (29) wykazali, że zawartość cukrów rozpuszczalnych, kwasów organicznych wzrasta wraz ze wzrostem dawki fal czerwonych. Podobne wyniki uzyskano w innych badaniach. Wyższą średnią masę owoców pomidora uzyskano w roślinach oświetlonych uzupełniająco lampami HPS w porównaniu z roślinami z lampami LED (8.7-12.2% w zależności od odmiany) (30).
Jednak badania Dzakovicha i in. (31) udowodnili, że dodatkowa jakość światła (HPSL przez diody LED) nie wpłynęła znacząco na właściwości fizykochemiczne (całkowita rozpuszczalna substancja stała, miareczkowalna kwasowość, zawartość kwasu askorbinowego, pH, całkowita zawartość związków fenolowych oraz znaczące flawonoidy i karotenoidy) ani właściwości sensoryczne pomidorów uprawianych w szklarni. To pokazuje, że na ilość cukrów rozpuszczalnych w owocach mogą wpływać nie tylko poszczególne czynniki, ale także ich kombinacje. Również w naszych eksperymentach nie udało się znaleźć prawidłowości między wpływami światła na zawartość kwasu. W szczególności przyszłe badania powinny koncentrować się nie tylko na relacji między gatunkiem a światłem, ale także na relacji między odmianą a światłem. Zawartość suchej masy była wyższa w „Chocomate F1” i „Strabena F1”. Odpowiada to Kurinie i in. (6), gdzie przeciętnie czerwono-brązowe przydziały gromadziły więcej suchej masy (6.46%). Badania Dumy i in. (32) wykazali, że porównując masę owoców i TI, obserwuje się, że wyższe TI dotyczy mniejszych lub większych pomidorów. Eksperymenty Rodica et al. (23) wykazały, że pomidory wiśniowe i brązowo-czerwone zawierają więcej rozpuszczalnych substancji stałych. W pracy podkreślono, że ilość związków organicznych decydujących o smaku owoców zależy od plonu odmiany.
Ekspozycja na dodatkowe czerwone i niebieskie oświetlenie LED zwiększa likopen i в-zawartość karotenu (13, 29, 33, 34). Dannehl i in. (12) Badania wykazały, że zawartość likopenu i luteiny w pomidorach była o 18 i 142% wyższa, gdy były one wystawione na działanie oprawy LED. Jednakże, в-zawartość karotenu nie różniła się między zabiegami świetlnymi. Ntagkas i in. (35) wykazali, że zeaksantyna, produkt в-konwersja karotenu, wzrasta w owocach pomidora w świetle niebieskim i białym. W tym badaniu twierdzenia te częściowo są prawdziwe tylko w przypadku „Bolzano F1”, gdzie stwierdzono znacznie większą ilość likopenu po obróbce LED, ale в-karoten zareagował negatywnie na to leczenie. Może to wynikać z cech genetycznych, ponieważ „Bolzano F1” jest w tym badaniu tylko odmianą o owocach pomarańczowych. W innych badaniach, z odmianami czerwono-owocowymi i brązowymi, największa ilość likopenu i в-karoten wykryto pod lampami indukcyjnymi, co nie potwierdza trendów z poprzednich lat (29). Nasze doświadczenia wykazały, że zawartość likopenu we wszystkich odmianach pomidora z czerwonymi owocami wzrastała wraz ze wzrostem światła niebieskiego. Natomiast zmiany zawartości karotenu w różnych odmianach nie pozwalają ustalić prawidłowości wspólnych dla wszystkich odmian pomidora użytych w doświadczeniach. Ta rozbieżność wskazuje na potrzebę dodatkowego testowania przedmiotu w przyszłości. Ten sam wzorzec odpowiedzi na światło ze względu na cechy odmiany zaobserwowano w przypadku ilości fenoli i flawonoidów. Wszystkie odmiany o czerwonych i brązowych owocach wykazały lepsze wyniki pod lampami IND, podczas gdy „Bolzano F1” zareagowało wyższymi wynikami na lampy HPSL i LED bez znaczącej różnicy. To badanie koresponduje z odkryciami Konga: leczenie niebieskim światłem znacząco doprowadziło do zwiększenia stężenia poszczególnych związków fenolowych (kwas chlorogenowy, kwas kawowy i rutyna) (16). Ciągłe światło czerwone znacznie zwiększyło likopen, в-karoten, całkowita zawartość fenoli, całkowite stężenie flawonoidów i aktywność przeciwutleniająca w pomidorach (36). W naszych wcześniejszych badaniach, flawonoidy zmieniały się jako fluktuacje; w związku z tym brak wpływu długości fali świetlnej należy uznać za znaczący.
Ilość fenoli wzrosła wraz ze wzrostem udziału światła niebieskiego dostarczanego przez lampy LED (29)odpowiada to również naszym badaniom. W pracach innych badaczy wspomina się, że ekspozycja na światło UV lub LED nie miała wpływu na całkowite związki fenolowe, mimo że wiadomo, że obie metody leczenia światłem modulują ekspresję szeregu genów zaangażowanych w biosyntezę związków fenolowych i karotenoidów (36). Należy wspomnieć, że podobnie jak w przypadku masy owocu, nie ma znaczących różnic w związkach chemicznych w „Encore F1” ze względu na obróbkę światłem. Pozwala to stwierdzić, że odmiana „Encore F1” może być tolerancyjna na skład światła. Nasze eksperymenty potwierdzają dane literaturowe, że synteza metabolitów wtórnych jest wzmocniona zarówno przez ilościową ilość światła niebieskiego, jak i zwiększony udział światła niebieskiego w całym systemie oświetlenia.
Uzyskane wyniki wskazują, że składniki chemiczne, w tym cukry rozpuszczalne w kwasach i ich proporcje, które odpowiadają za charakterystyczny smak odmiany, zależą przede wszystkim od genetyki odmiany. Dobry smak pomidorów charakteryzuje się nie tylko połączeniem specyficznych gatunkowo pigmentów i substancji biologicznie czynnych, ale także ich ilością. W szczególności stosunek i ilość kwasów i cukrów charakteryzują nasycony i wysokiej jakości smak. W tym badaniu dodatnia korelacja między cukrami rozpuszczalnymi a kwasami miareczkowanymi wynosi ~0.4, co jest skorelowane z badaniami Hernandeza Suareza, gdzie stwierdzono dodatnią korelację między dwoma wskaźnikami na poziomie 0.39. (37). W badaniach Dzakovich et al. (31), pomidory sprofilowano pod kątem całkowitej rozpuszczalnej substancji stałej, miareczkowej kwasowości, zawartości kwasu askorbinowego, pH, sumy fenoli oraz znaczących flawonoidów i karotenoidów. Ich badania wykazały, że na jakość owoców pomidora szklarniowego miała tylko marginalny wpływ dodatkowe zabiegi świetlne. Co więcej, dane z panelu sensorycznego konsumentów wykazały, że pomidory wyhodowane przy różnych zabiegach oświetleniowych były porównywalne w testowanych zabiegach oświetleniowych. Badanie zasugerowało, że dynamiczne środowisko świetlne właściwe dla systemów produkcji szklarniowej może zniwelować wpływ długości fal światła wykorzystywanych w badaniach na określone aspekty metabolizmu wtórnego owoców (31). Częściowo jest to zgodne z tym badaniem, ponieważ uzyskane liczby nie pokazują wyraźnych i jednoznacznych trendów, co pozwala stwierdzić, że jedno oświetlenie jest bardziej przydatne dla pomidorów niż inne. Jednak niektóre lampy mogą być używane dla niektórych odmian, na przykład lampy HPSL byłyby bardziej odpowiednie dla „Bolzano F1”, a oświetlenie LED jest zalecane dla „Chocomate F1”. Odpowiada to badaniom, w których badano wpływ różnych szerokości geograficznych na właściwości chemiczne pomidorów. Bhandari et. (38) wyjaśnił, że chociaż połączenie położenia słońca względem nieba, a w konsekwencji połączenie widzialnych fal świetlnych, odgrywa ważną rolę w zmianie składu chemicznego pomidorów; istnieją odmiany odporne na te procesy. Wszystkie te wnioski pozwalają podkreślić, że skład chemiczny pomidora zależy przede wszystkim od genotypu, gdyż związki odmian z czynnikami wzrostu, zwłaszcza z oświetleniem, są predysponowane genetycznie.
WNIOSEK
Różne odmiany pomidorów różnie reagują na zastosowane oświetlenie dodatkowe. Odmiany „Encore” i „Strabena” są najbardziej niewrażliwe na dodatkowe światło. W przypadku „Encore” jedynym parametrem, na który znacząco wpływa widmo światła LED, jest zawartość rozpuszczalnych substancji stałych. „Strabena” jest również stosunkowo tolerancyjna na zmiany składu spektralnego światła. Mogło to wynikać z cech genetycznych odmiany, gdyż była to jedyna odmiana pomidora koktajlowego uwzględniona w doświadczeniu. Nie zaleca się uprawy owoców koloru pomarańczowego cv „Bolzano” pod lampą LED lub IND, ponieważ w tym oświetleniu parametry są na poziomie HPSL lub znacznie gorsze. Pod lampami LED waga jednego owocu, suchej masy, zawartości rozpuszczalnych substancji stałych i в-karoten są znacznie zredukowane. Waga jednego owocu i ilość в-karoten o kolorze czerwono-brązowym owoców cv „Czekoladowy” pod oświetleniem LED znacznie wzrasta. Pozostałe parametry wykluczone z suchej masy oraz zawartość rozpuszczalnych substancji stałych są również wyższe niż w owocach uzyskanych z HPSL.
Eksperymenty wykazały, że HPSL stymuluje akumulację metabolitów pierwotnych w owocach pomidora. We wszystkich przypadkach zawartość rozpuszczalnych substancji stałych była o 4.7-18.2% wyższa w porównaniu z innymi źródłami światła.
Ponieważ lampy LED i IND emitują około 20% niebiesko-fioletowego światła, wyniki sugerują, że ta część widma stymuluje akumulację związków fenolowych w owocach o 1.6-47.4% w porównaniu z HPSL. Zawartość karotenoidów jako metabolitów wtórnych zależy zarówno od odmiany, jak i źródła światła. Odmiany czerwonych owoców mają tendencję do większej syntezy в-karoten pod dodatkowym światłem LED i IND.
Niebieska część spektrum odgrywa większą rolę w zapewnianiu jakości upraw. Wzrost lub kwantyfikacja jego udziału w całym widmie sprzyja syntezie metabolitów wtórnych (likopenu, fenoli i flawonoidów), prowadząc do zmniejszenia zawartości suchej masy i rozpuszczalnych substancji stałych.
Biorąc pod uwagę duży wpływ zmienności genotypowej na pomidory i relacje świetlne, dalsze badania powinny nadal koncentrować się na kombinacjach odmian i różnych uzupełniających widmach światła w celu zwiększenia zawartości związków biologicznie czynnych.
OŚWIADCZENIE O DOSTĘPNOŚCI DANYCH
Surowe dane uzasadniające wnioski z tego artykułu zostaną udostępnione przez autorów bez zbędnych zastrzeżeń.
AUTORSKIE WKŁADY
IE była odpowiedzialna za hodowlę i pobieranie próbek pomidorów, prace laboratoryjne, kwantyfikację związków, a także przyczyniła się do napisania manuskryptu. IA wpadła na pomysł, wniosła wkład w koncepcję i projekt badania, była odpowiedzialna za pobieranie próbek pomidorów, prace laboratoryjne, kwantyfikację związków, a także przyczyniła się do napisania manuskryptu. MD przyczynił się do opracowania koncepcji i projektu badania, optymalizacji metod analitycznych, przeanalizował próbki w laboratorium oraz przedstawił zalecenia i sugestie. RA wniósł wkład w analizę statystyczną, interpretację danych oraz przedstawił zalecenia i sugestie dotyczące manuskryptu. LD przyczynił się do opracowania koncepcji i projektu badania, był odpowiedzialny za pobieranie próbek pomidorów, prace laboratoryjne, kwantyfikację związków oraz przedstawiał zalecenia i sugestie dotyczące rękopisu. Wszyscy autorzy przyczynili się do powstania artykułu i zatwierdzili przedłożoną wersję manuskryptu.
FUNDUSZ
Niniejsze badanie zostało sfinansowane ze środków Łotewskiego Programu Rozwoju Obszarów Wiejskich 2014-2020 Współpraca, konkurs 16.1 projekt Nr. 19-00-A01612-000010 Badanie innowacyjnych rozwiązań i opracowanie nowych metod zwiększania wydajności i jakości w łotewskim sektorze szklarniowym (IRIS).
LITERATURA
- 1. Vijayakumar A, Shaji S, Beena R, Sarada S, Sajitha Rani T, Stephen R i in. Wywołane wysoką temperaturą zmiany parametrów jakościowych i plonu pomidora (Solanum lycopersicum L) oraz współczynniki podobieństwa między genotypami za pomocą znaczników SSR. Helion. (2021) 7:e05988. doi: 10.1016/j.heliyon.2021.e0 5988
- 2. Duzen IV, Oguz E, Yilmaz R, Taskin A, Vuruskan A, Cekici Y, et al. Likopen ma działanie ochronne na uszkodzenie serca wywołane wstrząsem septycznym u szczurów. Bratisl Med J. (2019) 120:919-23. doi: 10.4149/BLL_2019_154
-
3. Dogukan A, Tuzcu M, Agca CA, Gencoglu H, Sahin N, Onderci M, et al. kompleks likopenu pomidorowego chroni nerki przed uszkodzeniem wywołanym cisplatyną poprzez wpływ na stres oksydacyjny, a także na Bax, Bcl-2 i HSP wyrażenie. Rak orzecha. (2011) 63:427-34. doi: 10.1080/01635581.2011.5 35958
- 4. Warditiani NK, Sari PMN, Wirasuta MAG. Fitochemiczny i hipoglikemiczny wpływ ekstraktu z likopenu pomidorowego (TLE). Sys Rev Pharm. (2020) 11:50914. doi: 10.31838/srp.2020.4.77
- 5. Ando A. „Związki smakowe w pomidorach”. W: Higashide T, redaktor. Solanum Lycopersicum: produkcja, biochemia i korzyści zdrowotne. Nowy Jork, Nova Science Publishers (2016). p. 179-187.
- 6. Kurina AB, Solovieva AE, Chrapalova IA, Artemyeva AM. Skład biochemiczny owoców pomidora o różnych kolorach. Vavilovskii Zhurnal Genet Selektsii. (2021) 25:514-27. doi: 10.18699/VJ21.058
- 7. Murshed R, Lopez-Lauri F, Sallanon H. Wpływ stresu wodnego na układy antyoksydacyjne i parametry oksydacyjne owoców pomidora (Solanum lycopersicon L, cvMicro-tom). Physiol Mol Biol Rośliny. (2013) 19:36378. doi: 10.1007/s12298-013-0173-7
- 8. Klunklin W, Savage G. Wpływ cech jakościowych pomidorów uprawianych w warunkach stresu dobrze nawodnionego i suszy. Żywność. (2017) 6:56. doi: 10.3390/żywność6080056
- 9. Chetelat RT, Ji Y. Cytogenetyka i ewolucja. Genetic Improv Uprawy Solanaceous. (2007) 2:77-112. doi: 10.1201/b10744-4
- 10. Wang W, Liu D, Qin M, Xie Z, Chen R, Zhang Y. Wpływ oświetlenia uzupełniającego na transport potasu i zabarwienie owoców pomidorów uprawianych w hydroponice. Int J Mol Sci. (2021) 22:2687. doi: 10.3390/ijms22052687
- 11. Ouzounis T, Giday H, Kj^r KH, Ottosen CO. LED czy HPS w ornamentach? Studium przypadku w różach i kampanulach. Eur J Hortic Sci. (2018) 83:16672. doi: 10.17660/eJHS.2018/83.3.6
- 12. Dannehl D, Schwend T, Veit D, Schmidt U. Wzrost wydajności, zawartości likopenu i luteiny w pomidorach uprawianych w ciągłym widmie PAR Oświetlenie ledowe. Przód Roślin Sci. (2021) 12:611236. doi: 10.3389/fpls.2021.61 1236
- 13. Xie BX, Wei JJ, Zhang YT, Song SW, Su W, Sun GW i in. Dodatkowe światło niebieskie i czerwone promuje syntezę likopenu w owocach pomidora. J Zintegruj Rolnictwo. (2019) 18:590-8. doi: 10.1016/S2095-3119(18)62062-3
- 14. Zhang JY, Zhang YT, piosenka SW, Su W, Hao YW, Liu HC. Dodatkowe czerwone światło powoduje wcześniejsze dojrzewanie owoców pomidora w zależności od produkcji etylenu. Środowisko Exp Bot. (2020) 175:10404. doi: 10.1016/j.enveexpbot.2020.104044
- 15. Zhang Y, Zhang Y, Yang Q, Li T. Dodatkowe, dalekosiężne światło nad głową stymuluje wzrost pomidorów przy oświetleniu wewnątrz baldachimu za pomocą diod LED. J Zintegruj Rolnictwo. (2019)18:62-9. doi: 10.1016/S2095-3119(18)62130-6
- 16. Kong D, Zhao W, Ma Y, Liang H, Zhao X. Wpływ oświetlenia diodą elektroluminescencyjną na jakość świeżo krojonych pomidorków koktajlowych w magazynowanie. Int J Food Sci Technol. (2021) 56: 2041-52. doi: 10.1111/ijfs. 14836
- 17. Jarqum-Enriquez L, Mercado-Silva EM, Maldonado JL, Lopez-Baltazar J. Szklarnia ma wpływ na zawartość i kolor likopenu pokrywa. Sc Ogrodnictwo. (2013) 155:43-8. doi: 10.1016/j.scienta.2013. 03.004
- 18. Wahid A, Gelani S, Ashraf M, Foolad MR. Tolerancja ciepła
w roślinach: przegląd. Środowisko Exp Bot. (2007) 61:199
223. doi: 10.1016/j.enveexpbot.2007.05.011
- 19. Duma M, Alsina I. Zawartość barwników roślinnych w papryce czerwonej i żółtej. Sci Pap B Ogrodnictwo. (2012) 56:105-8.
- 20. Nagata M, Yamashita I. Prosta metoda jednoczesnego oznaczania chlorofilu i karotenoidów w owocach pomidora. Jpn Food Sci Technol. (1992) 39:925-8. doi: 10.3136/nskkk1962.39.925
- 21. Singleton VL, Orthofer R, Lamuela-Raventos RM. Analiza fenoli całkowitych i innych substratów utleniania oraz przeciwutleniaczy za pomocą odczynnika folin-ciocalteu. Metody Enzymol. (1999) 299:152-78. doi: 10.1016/S0076-6879(99)99017-1
- 22. Kim D, Jeond S, Lee C. Zdolność przeciwutleniająca fenolowych fitochemikaliów z różnych odmian śliwek. Chemia Spożywcza (2003) 81:321-6. doi: 10.1016/S0308-8146(02)00423-5
- 23. Rodica S, Maria D, Alexandru-Ioan A, Marin S. Ewolucja niektórych parametrów odżywczych owoców pomidora w okresie etapy zbiorów. Hort Sci. (2019) 46:132-7. doi: 10.17221/222/2017-HORTCI
- 24. Mate MD, Szalokine Zima I. Rozwój i plon pomidora polowego przy różnym zaopatrzeniu w wodę. Res J Rolnictwo Sci. (2020) 52:167-77.
- 25. Mauxion JP, Chevalier C, Gonzalez N. Złożone zdarzenia komórkowe i molekularne określające wielkość owoców. Trendy Roślin Sci. (2021) 26:1023-38. doi: 10.1016/j.trośliny.2021.05.008
- 26. Olle M, Alsina I. Wpływ długości fali światła na wzrost, plon i jakość odżywczą warzyw szklarniowych. Proc Łotewski Acad Sci B. (2019) 73:1-9. doi: 10.2478/prolas-2019-0001
- 27. Kawaguchi K, Takei-Hoshi R, Yoshikawa I, Nishida K, Kobayashi M, Kushano M i in. Funkcjonalne zakłócenie działania inhibitora inwertazy ściany komórkowej poprzez edycję genomu zwiększa zawartość cukru w owocach pomidora bez zmniejszyć wagę owoców. Sci Rep. (2021) 11:1-12. doi: 10.1038/s41598-021-00966-4
- 28. Olle M, Virsile A. Wpływ długości fali światła na wzrost, plon i jakość odżywczą warzyw szklarniowych. Rolnictwo Nauka o Żywności. (2013) 22:22334. doi: 10.23986/afsci.7897
- 29. Erdberga I, Alsina I, Dubova L, Duma M, Sergejeva D, Augspole I i in. Zmiany składu biochemicznego owoców pomidora pod wpływem jakości oświetlenia. Klucz Eng Mater. (2020) 850:172
- 30. Gajc-Wolska J, Kowalczyk K, Metera A, Mazur K, Bujalski D, Hemka L. Wpływ oświetlenia uzupełniającego na wybrane parametry fizjologiczne i plonowanie roślin pomidora. Folia Horticulturae. (2013) 25:153
-
9. doi: 10.2478/fhort-2013-0017
- 31. Dzakovich M, Gomez C, Ferruzzi MG, Mitchell CA. Właściwości chemiczne i sensoryczne pomidorów szklarniowych pozostają niezmienione w odpowiedzi na czerwone, niebieskie i dalekie czerwone światło dodatkowe emitowane przez światło. Hortnauka. (2017) 52: 1734-41. doi: 10.21273/HORTSC12469-17
- 32. Duma M, Alsina I, Dubova L, Augspole I, Erdberga I. Sugestie dla konsumentów dotyczące przydatności różnokolorowych pomidorów w żywieniu. W:
FoodBalt 2019: Materiały 13. Bałtyckiej Konferencji Nauki o Żywności i Technologii; 2019 2-3 maja. Jełgawa, Łotwa: LLU (2019). p. 261-4.
- 33. Ngcobo BL, Bertling I, Clulow AD. Oświetlenie przed zbiorami pomidorów koktajlowych skraca okres dojrzewania, poprawia koncentrację karotenoidów w owocach i ogólną jakość owoców. J Hortic Sci Biotechnol. (2020) 95:617-27. doi: 10.1080/14620316.2020.1743771
- 34. Najera C, Guil-Guerrero JL, Enriquez LJ, Alvaro JE, Urrestarazu
M. Wzmocnione diodami LED właściwości dietetyczne i organoleptyczne w
owoce pomidora po zbiorze. Pożniwny Biol Technol. (2018)
145:151-6. doi: 10.1016/j.postharvbio.2018.07.008
- 35. Ntagkas N, de Vos RC, Woltering EJ, Nicole C, Labrie C, Marcelis LF. Modulacja metabolomu owoców pomidora za pomocą światła LED. Metabolity. (2020) 10:266. doi: 10.3390/metabo10060266
- 36. Baenas N, Iniesta C, Gonzalez-Barrio R, Nunez-Gomez V, Periago MJ, Garda-Alonso FJ. Stosowanie po zbiorach światła ultrafioletowego (UV) i diody elektroluminescencyjnej (LED) w celu wzmocnienia związków bioaktywnych w chłodzone pomidory. Cząsteczki. (2021) 26:1847. doi: 10.3390/molekuły 260 71847
- 37. Hernandez Suarez M, Rodriguez ER, Romero CD. Analiza zawartości kwasów organicznych w odmianach pomidora zebranego na Teneryfie. Eur Food Res Technol. (2008) 226:423-35. doi: 10.1007/s00217-006-0553-0
- 38. Bhandari HR, Srivastava K, Tripathi MK, Chaudhary B, Biswas S. Shreya Environmentx Łączenie interakcji zdolności dla cech jakościowych pomidora (Solanum lycopersicum L.). Int J Bio-Resour Stress Management. (2021) 12:455-62. doi: 10.23910/1.2021.2276
Konflikt interesów: Autorzy deklarują, że badanie zostało przeprowadzone przy braku jakichkolwiek powiązań handlowych lub finansowych, które mogłyby być odebrane jako potencjalny konflikt interesów.
Uwaga wydawcy: Wszystkie twierdzenia wyrażone w tym artykule są wyłącznie twierdzeniami autorów i niekoniecznie reprezentują twierdzenia ich stowarzyszonych organizacji lub wydawcy, redaktorów i recenzentów. Żaden produkt, który może być oceniany w tym artykule, lub twierdzenie, które może być wystawione przez jego producenta, nie jest gwarantowane ani popierane przez wydawcę.
Copyright © 2022 Alsina, Erdberg, Duma, Alksnis i Dubova. Jest to artykuł o otwartym dostępie rozpowszechniany na warunkach licencji Creative Commons Attribution License (CC BY).
Nowe możliwości w dziedzinie żywienia | www.frontiersin.org